在化学的世界里,方程式是描述化学反应的“语言”。它们以简洁明了的方式,展现了反应物转化为生成物的过程。今天,我们将一起探索如何书写红磷燃烧的化学方程式,这一过程不仅涉及到化学方程式的基本构成,还涵盖了化学反应类型的识别、配平技巧以及化学方程式的意义等多方面内容。
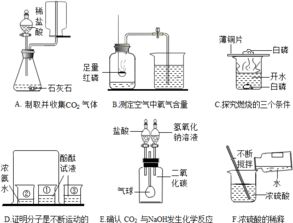
化学方程式是化学反应的符号表示,它遵循质量守恒定律,即反应前后物质的总质量保持不变。一个完整的化学方程式包括反应物和生成物,用等号“=”或箭头“→”连接。反应物位于等号的左侧,表示反应开始时的物质;生成物位于等号的右侧,表示反应结束后的新物质。在方程式中,各物质的化学式下方有时会标注系数,代表参与反应的分子或原子的数量。
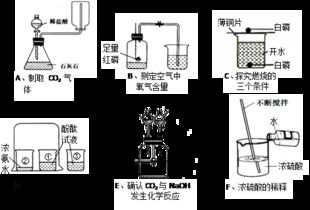
红磷,一种化学元素磷的同素异形体,以其鲜艳的红色和较低的燃点著称。在空气中,红磷可以自发地与氧气发生燃烧反应,释放出大量的热和光。这一过程是典型的氧化反应,即物质与氧结合,生成氧化物。红磷燃烧的主要产物是五氧化二磷(P₂O₅),这是一种白色固体,具有强烈的吸湿性。

首先,明确反应涉及的所有物质。在红磷燃烧的例子中,反应物是红磷(P)和氧气(O₂),生成物是五氧化二磷(P₂O₅)。
根据反应物和生成物,初步写出化学方程式。此时不考虑系数的平衡,仅列出物质的基本化学式。例如:
P + O₂ → P₂O₅
配平是确保化学方程式满足质量守恒定律的关键步骤。配平的目标是使得反应物和生成物中每种元素的原子总数在反应前后保持一致。对于红磷燃烧的反应,我们可以这样配平:
观察磷元素,P在左侧单独存在,而在右侧以P₂形式出现,因此左侧P的系数应设为2,以保持磷原子数量平衡。
接着考虑氧元素,O在左侧以O₂形式存在,而在右侧每个P₂O₅分子中含有5个O原子。为了平衡氧原子,我们可以尝试将O₂的系数设为2.5(因为5/2=2.5,每个P₂O₅需要5个O原子,而每个O₂提供2个O原子),但化学方程式中的系数应为整数。这里,我们需要将整个方程式扩大两倍以消除小数,即P的系数变为4,O₂的系数变为5,P₂O₅的系数变为2。
经过配平,我们得到:
4P + 5O₂ → 2P₂O₅
这就是红磷燃烧的正确化学方程式。
最后,检查方程式以确保所有元素的原子数在反应前后平衡。对于上述方程式,左侧有4个磷原子和10个氧原子,右侧同样有4个磷原子(2个P₂分子)和10个氧原子(2个P₂O₅分子),满足质量守恒定律。
化学方程式不仅仅是化学反应的符号记录,它们还承载着丰富的信息。通过分析化学方程式,我们可以了解:
反应类型:红磷燃烧属于化合反应,即两种或多种物质结合形成一种新物质。
反应条件:虽然化学方程式本身不直接显示反应条件(如温度、压力),但我们知道红磷燃烧通常需要在空气中点燃。
能量变化:燃烧反应伴随着能量的释放,红磷燃烧产生光和热,是典型的放热反应。
物质性质:通过方程式,我们可以推断出反应物和生成物的化学性质,如红磷的可燃性和五氧化二磷的稳定性。
配平化学方程式是化学学习中的难点之一,但掌握一些技巧可以大大简化这一过程:
观察法:从复杂或特殊的原子团开始配平,如本题中的P₂O₅,先确定磷的系数,再根据氧原子数量调整氧气系数。
奇数配偶法:若某元素的原子在方程式两边出现的次数较多,且一边的原子数为奇数,可先将该元素的原子数配成偶数,再逐步配平其他元素。
代数法:对于更复杂的反应,可以设立代数方程来求解各物质的系数。
检查法:配平后务必检查,确保所有元素的原子总数在反应前后完全一致。
书写红磷燃烧的化学方程式是一个结合了化学知识、逻辑思维和数学技巧的过程。通过明确反应物和生成物、初步写出方程式、配平、检查等步骤,我们可以准确地描述这一化学反应。更重要的是,化学方程式不仅是化学反应的记录,更是理解物质性质、反应类型、能量变化等化学核心概念的重要工具。希望本文能帮助读者更好地掌握书写化学方程式的方法,激发对化学世界的探索兴趣。
72.76M周公解梦大全2345原版
60.38M活力充电
66M哮天犬容器科技
53.83M小鸟电视
29.81M病娇模拟器旧版
54.92M万能遥控器大师极速版
9.66M病娇模拟器同人1.5.6版本
69.39M速影TV电视版
21.08M旅行翻译官
85.45M南充一卡通
本站所有软件来自互联网,版权归原著所有。如有侵权,敬请来信告知 ,我们将及时删除。 琼ICP备2024021917号-10